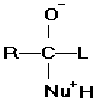
SOSTITUZIONE NUCLEOFILA
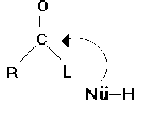
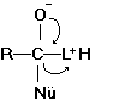
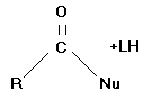
Tale reazione riguarda i gruppi acilici. Il nucleofilo, una specie ricca di elettroni, legato ad un idrogeno è in grado di attaccare il carbonio (con carica d+) e di legarsi con esso; di conseguenza il doppio legame con l’ossigeno si rompe e diventa semplice, l’ossigeno, da una parziale carica negativa d-, acquista una carica negativa completa, il nucleofilo acquista invece una carica positiva. In seguito l’idrogeno legato al nucleofilo si lega al gruppo L e il nucleofilo perde la carica positiva che è invece acquistata da L. A questo punto la carica negativa dell’ossigeno ritorna sul carbonio ristabilendo il doppio legame, si scinde il legame di C con L, L si stacca perdendo la carica positiva. Quindi il prodotto della reazione sarà un nuovo derivato acilico con in più un gruppo uscente. Nel corso della reazione si è passati dalla struttura trigonale piana del primo gruppo acilico, alla struttura tetraedrica con il legame del nucleofilo per ritornare alla struttura trigonale del gruppo acilico.
 |
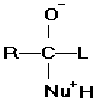 |
 |
 |
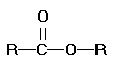
Come già detto gli esteri sono dei derivati acilici così formati:
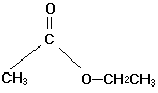
Un particolare estere
è l’acetato di etile
che deriva da una
reazione di sostituzione nucleofila
fra l’acido acetico e l’etanolo:
acetato di etile
L’acido acetico è una molecola polarizzata in cui il
carbonio ha una parziale carica d+ e l’ossigeno una parziale carica d- . L’etanolo funziona da
nucleofilo attaccando il carbonio dell’acido acetico e legandosi ad esso con
l’ossigeno del gruppo ossidrile il quale acquisterà una carica positiva. Allo
stesso tempo il doppio legame del carbonio con l’ossigeno del gruppo carbonilico
diventa semplice e l’ossigeno acquista una carica negativa completa. A questo
punto l’idrogeno del gruppo ossidrile dell’etanolo si lega al gruppo OH
dell’acido acetico che diventa OH2 con una carica positiva, mentre
l’ossigeno dell’etanolo ha perso la sua carica positiva. Ora l’ossigeno con
carica negativa riforma il doppio legame con il carbonio perdendo la carica
mentre il gruppo OH2 si stacca formando una molecola d’acqua. In
questo modo si hanno come prodotti di reazione l’acetato di etile e H2O.
Per accelerare la reazione si può eliminare l’acqua man
mano che si forma. La reazione di esterificazione è reversibile, la sua
reazione inversa prende il nome di idrolisi
degli esteri.
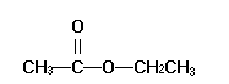
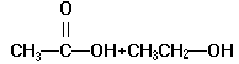
![]()
![]()
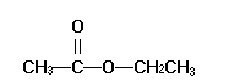
![]()
acido
acetico
alcool etilico
acqua
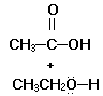
![]()
![]()
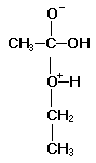
![]()
![]()
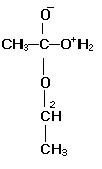
![]()
![]()
![]()
Indice di tutte le pagine del sito